Partager la publication "L’énigme de l’eau"
Par Jean de Pontcharra
Jean de Pontcharra1
Résumé : Quelques réflexions sur les surprenantes propriétés de l’eau nous montrent les difficultés des scientifiques à approcher l’essence des choses au moyen de leurs modèles basés sur les mathématiques, la mécanique, la physique ou la chimie. Les scientifiques se heurtent toujours à la même difficulté : ils veulent étendre le domaine des sciences à toute connaissance, même inaccessible à leurs appareils de mesure, au prix de spéculations non-scientifiques. L’eau n’est pas qu’un élément inerte, modélisable par quelques équations, fussent-elles très compliquées. Son action est liée de façon très complexe aux trois autres éléments : feu (chaleur), air (vapeur d’eau) et terre (cycle de l’eau).
Introduction :
Plus de dix mille publications, plus de 50 millions de pages internet par an, le thème de l’eau est inépuisable. La communauté scientifique internationale dépense des sommes considérables pour rechercher et expliquer les propriétés surprenantes de l’eau. Les modèles proposés sont innombrables et se contredisent souvent.
Le CNRS avait classé « les mystères de l’eau » en première place des énigmes scientifiques dans le cadre de l’année mondiale de la Physique 2005, avant les paradoxes quantiques, l’absence d’anti-matière ou la masse manquante de l’univers. En fait, ces paradoxes proviennent de notre approche matérialiste du réel : nos modèles sont trop grossiers et inadaptés à la perfection du cosmos. Et il n’y a aucune garantie qu’ils correspondent à la réalité (le cas du big-bang en est un exemple). Leur caractère explicatif et prédictif n’est que partiel et leurs insuffisances sont la conséquence de notre vision mécaniciste des phénomènes.
Dans la suite de cet article, le modèle atomique et moléculaire bien connu sera utilisé, tout en ayant conscience de ses limitations et en sachant qu’un modèle ondulatoire pourrait aussi être utilisé.
Généralités :
L’eau est le support d’une multitude de symboles matériels et spirituels, de bénédiction (maintien de la vie, purification, stabilisation du climat terrestre, échanges micro et macroscopiques, réactions chimiques), mais aussi de malédiction (inondations et érosion, Déluge, tsunamis). Elle est présente dans l’atmosphère, sur toute la surface de la terre, en grande majorité dans les océans et mers, mais aussi, d’après des découvertes récentes, dans la croûte et le manteau terrestre, et ce en quantités très importantes.
Étant un solvant universel, l’eau se charge des ions présents dans les matériaux qu’elle rencontre. Sans l’état gazeux sous forme de vapeur (distillation), ni l’état solide sous forme de glace, il n’y aurait pas d’eau douce sur terre. Et sans eau douce, point de vie.
Les propriétés de l’eau :
L’eau est unique : seul corps présent à la fois sous les états solide, liquide et gazeux dans les conditions de température et pression que l’on peut rencontrer à la surface de la terre, son comportement est surprenant et ne ressemble à celui d’aucun autre élément connu. Sa masse volumique à l’état liquide, lorsqu’elle est ultra-pure, est maximale : 1,0000 kg/l à T=3,98 °C à la pression atmosphérique standard ; 0,99984 kg/l à T=0°C ; 0,99565 kg/l à T=30°C ; 0,95840 à T=100°C.
Il y a un point sur le diagramme (pression P, température T) nommé point triple où l’eau se trouve dans les trois états : T=0,01°C et P= 611,2 Pa2.
Il existe un point critique à T=374 °C et P=22 MPa3 au-dessus duquel l’eau est dite « supercritique ». Bien que d’apparence liquide, l’eau acquiert alors des propriétés proches de celles des gaz et solubilise très bien les molécules de poids élevé. Cet état existe dans les profondeurs de la croûte et du manteau terrestres et intervient dans la cristallisation fractionnée de cristaux au sein des magmas liquides, ce qui bouleverse les connaissances actuelles des géophysiciens et des vulcanologues.
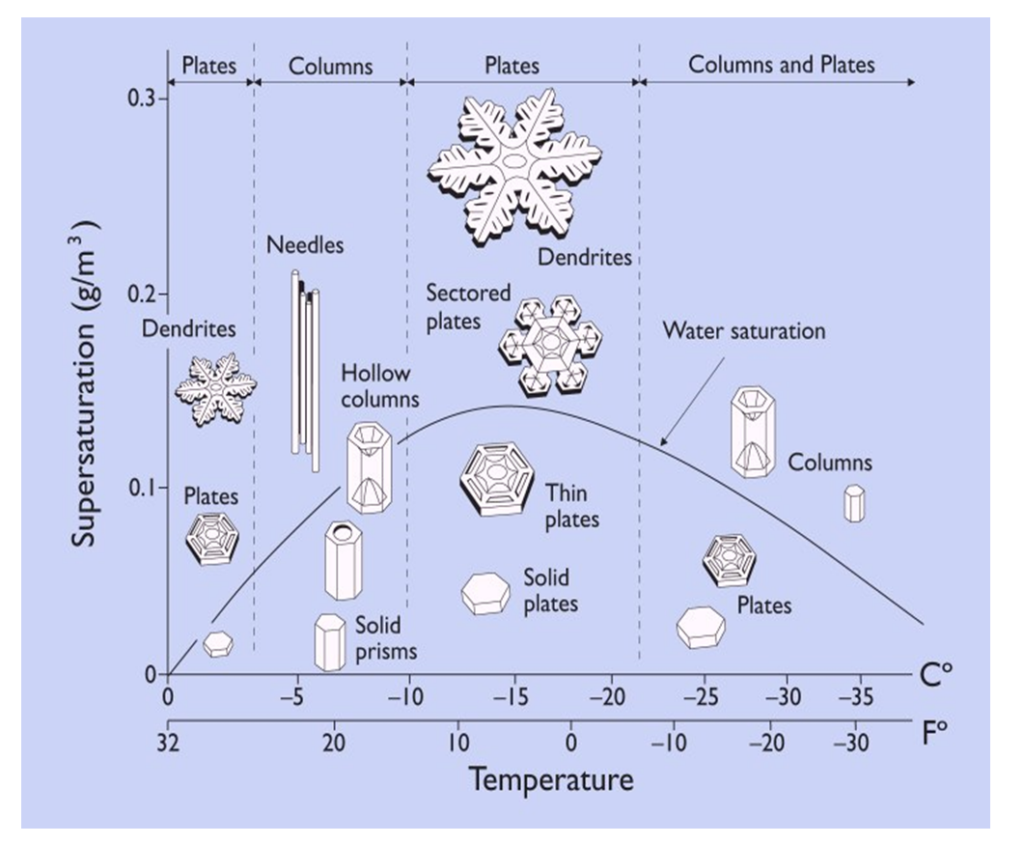
Fig. 1: Variétés possibles de cristaux de glace (Glace « ordinaire » hexagonale)
Les chiffres précédents sont valables pour une eau avec un taux d’impuretés très faible. L’eau pouvant dissoudre une grande quantité de corps, les résultats varient en fonction du pourcentage de ces corps dans l’eau. Par exemple, l’eau de mer salée à 35g/l gèle à plus basse température que l’eau pure.
La glace solide cristalline (glace hexagonale) a une densité inférieure à l’eau liquide : 0,917. Nommée glace « ordinaire », c’est elle qui constitue les cristaux de glace des flocons de neige.
L’exploration d’une gamme plus large de températures et pressions a mis en évidence plus de 15 formes différentes de glace cristalline et 3 formes amorphes. Par exemple, on trouve une glace amorphe plus lourde que le liquide et de densité 1,17 à T=-146°C et P=1,2 GPa4.
Le diagramme ci-dessous montre quelques structures observables et les conditions de transition associées, dans l’état actuel de nos connaissances.
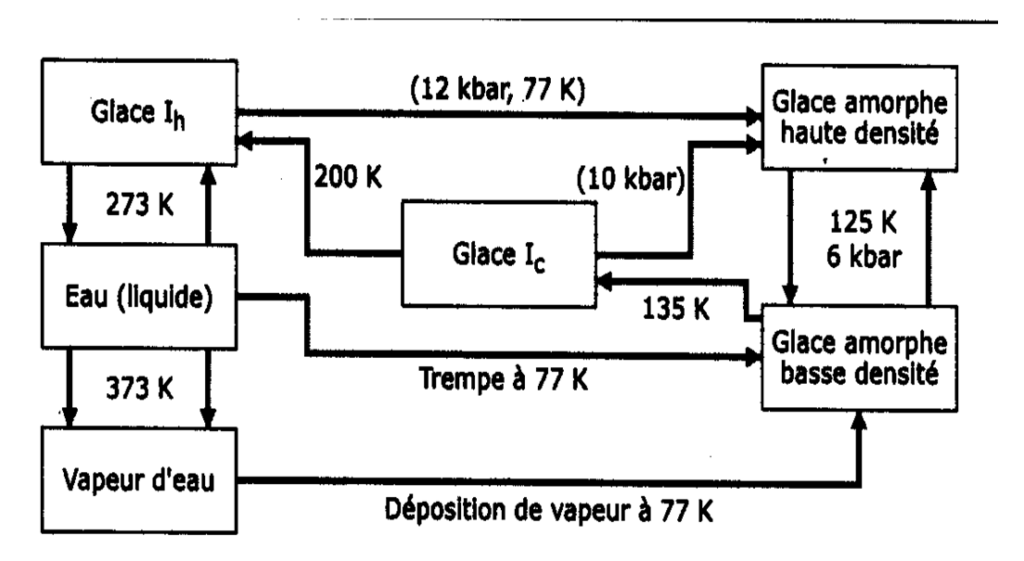
Fig. 2 : Quelques états instables de l’eau. Conversion : 0°C= 273°K.
Le bar vaut 105 pascals.
État de surfusion : si l’on « trempe » de l’eau ultra-pure en abaissant très rapidement sa température, elle reste liquide jusqu’à –40°C.
État de surchauffe : l’eau peut être chauffée à 220°C sans bouillir, si elle ne contient absolument aucune impureté.
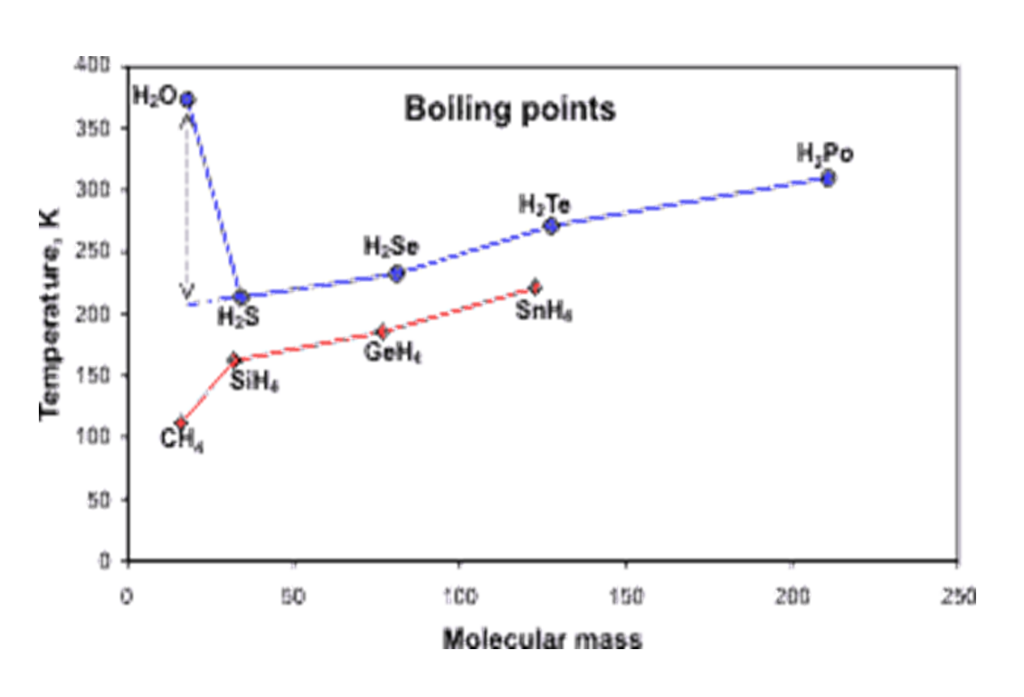
Fig. 3 : Températures d’ébullition de quelques liquides en fonction de leur poids moléculaire. L’extrapolation de la courbe aurait donné Te=-80°C (donc au-dessous de zéro) pour l’eau. Il n’y aurait alors que de la vapeur d’eau sur la terre, et toute forme de vie serait impossible.
La molécule d’eau.
La liaison hydrogène, concept lié au modèle atomique, expliquerait certaines propriétés macroscopiques de l’eau, mais pas toutes. L’énergie de liaison hydrogène entre 2 molécules d’eau différentes est plus faible que dans la liaison covalente O-H à l’intérieur de la même molécule.
La molécule d’eau H-O-H constitue un nano-résonateur qui peut entrer en vibration par excitation d’ondes externes. Des rayonnements énergétiques (UV, radiations) peuvent « casser » ces liaisons. L’agitation thermique rend ces liaisons plus fragiles.
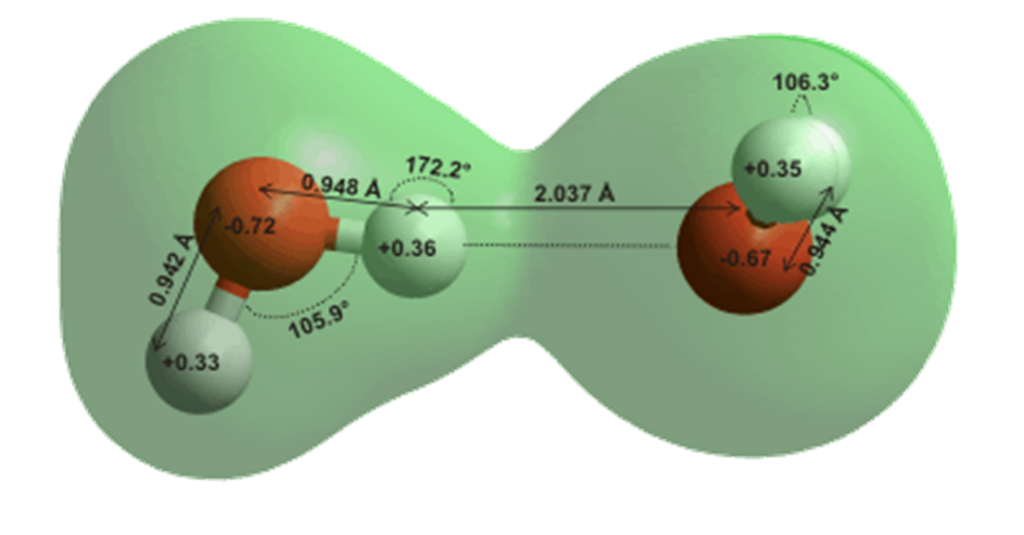
Fig. 4 : Modèle de dimère avec la liaison hydrogène, entre l’atome d’hydrogène de la molécule d’eau (à gauche du dessin) et l’atome d’oxygène de la molécule d’eau adjacente (à droite). L’angle H-O-H du monomère (1 molécule d’eau isolée) peut varier de 104,5° à 109,5°. Dans le dimère présenté ici, l’angle vaut 105.9° pour la molécule fournissant l’atome H, 106,3° pour la molécule fournissant l’atome O. La distance de centre à centre H-O de la liaison hydrogène n’est que de 0,2 nm.
Les hypothèses :
Les propriétés « anormales » de l’eau sont attribuées à la liaison hydrogène qui se crée entre un hydrogène d’une molécule d’eau et l’oxygène d’une molécule d’eau voisine. Chaque molécule d’eau peut ainsi s’associer à 4 voisines Le temps de rémanence de cette liaison est estimé à 1 ps1, temps extrêmement bref.
L’eau liquide est un assemblage dynamique se faisant et se défaisant très rapidement et pouvant inclure des îlots d’agglomérats ordonnés de plusieurs dizaines à plusieurs milliers de molécules, qui ont un temps de rémanence indépendant de celui de la liaison hydrogène, mais du même ordre de grandeur. Certains auteurs ont proposé une explication : l’eau serait le mélange de structures ordonnées semblables à celle de la glace, entourées de molécules plus mobiles, l’ensemble se modifiant sans cesse. De plus les atomes peuvent osciller autour de leur position, ce qui fait varier l’énergie de liaison.
Mais même les modèles les plus sophistiqués ne rendent pas compte de toutes les propriétés de l’eau. Par exemple la structure de l’eau est inconnue entre –40°C et –130°C. L’expérimentation et l’interprétation des résultats sont compliquées par le fait que l’eau pure n’existe que dans la pensée des chercheurs ou dans les programmes des ordinateurs.
La « catastrophe » de l’entropie :
Cette expression des physiciens recouvre le fait que l’eau liquide possède une entropie2 plus faible que la glace, ce qui semble contredire la 2ème loi de la thermodynamique. Les physiciens considèrent que le liquide est plus désordonné; donc son entropie devrait être plus grande. En fait, l’eau liquide contient plus d’information que la glace figée. Le niveau d’ordre de l’eau liquide ne peut pas être quantifié dans l’état actuel de nos connaissances, d’où le paradoxe apparent de l’entropie « catastrophique ».
L’eau dans l’organisme :
Il ne faut pas oublier qu’au sein des cellules vivantes l’eau est dans un espace confiné, où l’influence des membranes et des interfaces est très importante, donnant un comportement différent et beaucoup plus compliqué que dans un volume de grande dimension par rapport à la taille de la molécule.
L’eau participe aux échanges cellulaires (osmose) et aux échanges avec l’extérieur du corps (transpiration, vapeur dans les poumons, absorption cutanée); elle se présente sous forme mobile dans les systèmes circulatoire et lymphatique, joue un rôle dans les cellules immunitaires, dans la formation et réparation de l’ADN, dans la synthèse des protéines, etc. L’eau est un solvant doux universel.
Les expériences du professeur Benveniste, chercheur à l’INSERM, sur la « mémoire de l’eau », reproduites maintes fois par d’autres chercheurs, sont toujours âprement contestées par la science « officielle »3. L’arrangement des molécules d’eau pourrait se faire en fonction de l’environnement dans lequel elles se trouvaient à un moment donné. Cette « structure » serait une signature, comme une empreinte pouvant être « lue » ultérieurement par notre organisme.
Conclusion :
Nous n’avons pas besoin d’aller bien loin pour nous émerveiller devant la perfection de la Création. La science fait des progrès considérables dans les techniques d’analyse et d’observation. Mais le chercheur s’aperçoit qu’il bute sur une complexité et une perfection qui dépassent ses capacités d’explication, surtout s’il se restreint aux schémas mentaux réducteurs issus de sa formation matérialiste et mécaniciste.
_________________________________________
Pour compléter ce court article, une lettre d’Hippolyte Bayard4 à D. Arago faisant allusion à l’eau, est intéressante et montre déjà deux conceptions antagonistes de la physique.
Monsieur Dominique François Arago
Académie des Sciences, Paris
Cosmos, 1er janvier 1840
Monsieur le Physicien, Monsieur l’Astronome,
Vous ne connaissez pas la nature de la matière, vous ne connaissez pas la nature de l’antimatière. Dans votre laboratoire de petit scientifique, vous croyez capturer les secrets du cosmos. Dans vos éprouvettes, en combinant l’hydrogène et l’oxygène, vous croyez comprendre les mystères de l’eau. L’œil sur le microscope, en regardant l’infinitésiment petit qui constitue notre corps, vous croyez comprendre les mystères de la vie. L’œil au télescope, en regardant l’infinitésiment lointain, vous croyez comprendre les secrets des astres. Mais les éléments du cosmos, Monsieur le scientifique, ne sont pas faits pour vos lentilles. Eau, Air, Terre, Feu ont des secrets que vous ne pourrez jamais comprendre. Les astres suivent une trajectoire insondable pour vous. Et savez-vous pourquoi ? Parce qu’ils dansent. Tout danse, monsieur le scientifique, et il ne vous est pas consenti de suivre cette danse. Et savez-vous pourquoi tout danse ? Parce que tout est musique, monsieur le scientifique, et tout obéit à son tour à une musique que vos oreilles ne peuvent pas saisir. Air, Eau, Terre, Feu sont de la musique. Et ils dansent la musique qu’ils sont eux-mêmes. La Vie que vous cherchez dans votre laboratoire et dans votre observatoire est une musique que vous ne pourrez jamais saisir.
Hippolyte Bayard
À rapprocher de ce qu’écrivait le P. Sertillanges dans son Catéchisme des incroyants (Flammarion, 1964, p. 15) :
«…Tout ici bas est forme, nombre, harmonie, répétition et rythme, danse et musique ; rien n’est matière inerte et aveugle.»
Le meilleur site sur la physique de l’eau est celui de l’Anglais M. Chaplin, mis à jour très fréquemment, mais demandant un niveau universitaire en physique-chimie.
http://www.martin.chaplin.btinternet.co.uk/index2.html
Plus accessible :
José Texeira, « Les Mystères de l’Eau », Techniques de l’Ingénieur RE-53, 2006
José Texeira, « L’étrange comportement de l’eau ultrafroide », Pour la Science n° 285, Juillet 2001
1 Docteur en Physique, Jean de Pontcharra est chercheur spécialiste de microélectronique au CEA (Commissariat à l’énergie atomique) à Grenoble.
2 Le Pascal, abréviation Pa, est l’unité internationale de pression produite par une force de 1 Newton uniformément répartie sur une surface de 1 mètre carré. L’ancienne unité, le bar, vaut 105 Pa. Une atmosphère (poids d’une colonne d’air à T=20°C au niveau de la mer, équivalente à une colonne de 760 mm de mercure) vaut 1,013×105 Pa.
3 MPa : mégapascal : 1 million de Pa
4 Gpa : Gigapascal : 1 milliard de Pa
1 ps : pico seconde, 10-12 secondes
2 L’entropie d’un système fermé est proportionnelle à son degré de désordre.
3 Ndlr. A noter toutefois que le Pr Luc Montagnier Prix Nobel 2008 de médecine, a rendu publiquement hommage, dans sa conférence de Lugano (Italie) du 27 octobre 2007, à Jacques Benveniste (1935-2004). Cf. le site internet: colombre.it/montagnier .
4 H. Bayard (1801-1887), inventeur du positif photographique direct, avait vu sa découverte négligée par Arago qui, dans ses comptes-rendus à l’Académie des Sciences, lui préféra Daguerre.
